化学中考中,盐和化肥是重要的考查内容,其相关的实验探究题更是考察学生综合能力的关键。本专题试题由一线名师精心整理,紧扣中考考点,旨在通过典型实验题目,帮助学生掌握盐的性质、化肥的鉴别与使用等核心知识,提升实验探究与问题解决能力。
一、 核心知识梳理
1. 盐的化学性质:
* 与某些金属反应(金属活动性顺序的应用)。
- 与酸反应(生成新盐和新酸)。
- 与碱反应(生成新盐和新碱)。
- 与某些盐反应(生成两种新盐)。
- 化肥的种类与作用:
- 氮肥:促进叶色浓绿,枝叶茂盛。
- 磷肥:促进根系发达,增强抗寒抗旱能力。
- 钾肥:促进茎秆粗壮,增强抗病虫害和抗倒伏能力。
- 复合肥料:同时含有两种或两种以上营养元素。
- 常见离子的检验:如Cl⁻、SO₄²⁻、CO₃²⁻、NH₄⁺等,这是鉴别盐和化肥成分的基础。
二、 精品试题精讲(节选)
【例题1】(物质鉴别题)
实验室有四种白色固体,分别是碳酸钠、硫酸钠、氯化钠和碳酸钙,请设计实验方案进行鉴别。
【参考答案与分析】
1. 物理方法:观察溶解性。取少量样品于试管中,加入足量水,振荡。不溶解的是碳酸钙。
2. 化学方法:
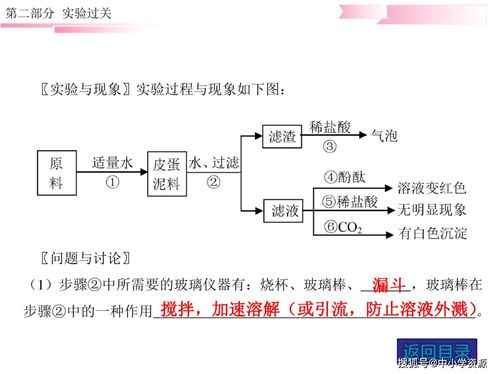
* 向三种溶液(或剩余固体加水后的上层清液)中分别滴加稀盐酸。产生气泡的是碳酸钠溶液。
- 向剩余两种溶液中分别滴加氯化钡溶液(或硝酸钡溶液),产生白色沉淀的是硫酸钠溶液(生成BaSO₄)。
- 无明显现象的是氯化钠溶液。
本题考点:盐的溶解性、碳酸盐与酸的反应、硫酸盐的检验。
【例题2】(实验探究题)
某农资商店有一包钾肥标签脱落,可能是氯化钾、硫酸钾或碳酸钾。请设计实验确定其成分。
【参考答案与分析】
1. 取少量样品于试管中,加入足量稀盐酸,若有气泡产生,则原样品为碳酸钾。
2. 若无气泡,则样品为氯化钾或硫酸钾。另取样品配成溶液,滴加几滴硝酸钡溶液,若产生白色沉淀(不溶于稀硝酸),则原样品为硫酸钾;若无明显现象,则为氯化钾。
本题考点:化肥种类鉴别、碳酸盐与酸的反应、硫酸根离子的检验。
【例题3】(综合应用题)
某同学在探究铵态氮肥(如NH₄Cl)性质时,发现其与碱性物质混合会释放出有刺激性气味的气体,导致肥效降低。请解释原因,并写出实验室检验铵根离子(NH₄⁺)的方法。
【参考答案与分析】
原因:铵盐能与碱反应生成氨气(NH₃),氨气逸出导致氮元素流失。例如:2NH₄Cl + Ca(OH)₂ → CaCl₂ + 2NH₃↑ + 2H₂O。因此,铵态氮肥不能与碱性物质(如草木灰,主要成分K₂CO₃)混合施用。
检验方法:取少量样品于试管中,加入氢氧化钠溶液,微热,将湿润的红色石蕊试纸靠近试管口。若试纸变蓝,则证明含有NH₄⁺。
本题考点:铵盐的性质、化肥的合理使用、NH₄⁺的检验。
三、 专题训练及答案(部分)
训练题1:如何鉴别氯化铵、硫酸铵和尿素【CO(NH₂)₂】三种氮肥?
答案要点:
1. 观察状态:尿素为白色颗粒状,另两种为晶体。
2. 取样加入碱液并加热,有氨味的是铵盐(氯化铵和硫酸铵),无氨味的是尿素。
3. 向两种铵盐溶液中分别滴加硝酸钡溶液,产生白色沉淀的是硫酸铵,另一种是氯化铵。
训练题2:设计实验证明某钾肥(主要成分为K₂SO₄)中是否混入了NH₄Cl。
答案要点:取少量样品于试管中,加入氢氧化钠溶液,微热,用湿润的红色石蕊试纸检验生成的气体。若试纸变蓝,则证明混有NH₄Cl;若不变蓝,则未混入。
四、 与备考建议
1. 夯实基础:牢记盐的溶解性表、常见离子的检验方法、化肥的种类与特性。
2. 掌握方法:熟练掌握物质鉴别、分离、提纯的实验设计思路,步骤清晰,现象描述准确。
3. 联系实际:关注化学知识与农业生产、环境保护的联系,如化肥的合理施用、铵态氮肥的保存等。
4. 规范表达:化学方程式书写规范,实验表述严谨,避免因表述不清而失分。
通过以上系统性的专题训练,结合对典型例题的深入剖析,考生能够有效构建关于盐和化肥的知识网络,提升解决中考化学实验探究类题目的能力,为取得优异成绩奠定坚实基础。自然科学的研究和试验发展,正是建立在这样严谨、求实的探究过程之上。